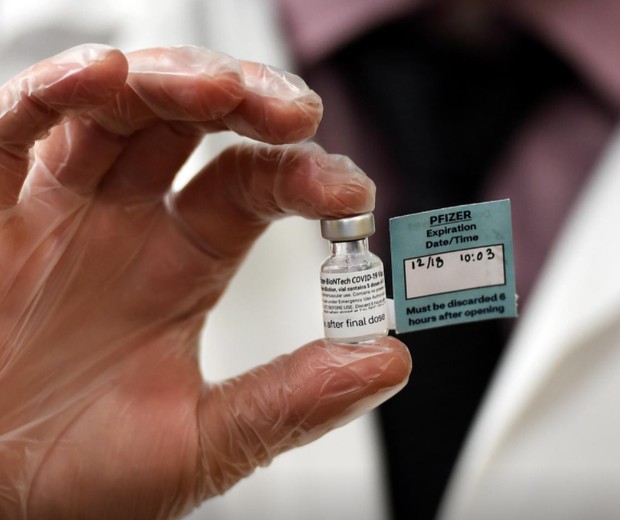
A Agência Nacional de Vigilância Sanitária (Anvisa) divulgou, nesta terça-feira (23), a concessão do registro definitivo da vacina contra a covid-19 produzida pela Pfizer - sendo esse o primeiro registro de vacina contra o novo coronavírus para uso amplo, nas Américas.
"O imunizante do Laboratório Pfizer/BioNTech teve sua segurança, qualidade e eficácia aferidas e atestadas pela equipe técnica de servidores da Anvisa que prossegue no seu trabalho de proteger a saúde do cidadão brasileiro. Esperamos que outras vacinas estejam em breve sendo avaliadas e aprovadas. Esse é o nosso compromisso", disse em nota o diretor-presidente da Anvisa, Antonio Barra Torres.
LEIA TAMBÉM: Quando a vacina contra a covid-19 estará disponível para crianças?
Segundo a Anvisa, o registro é emitido após 17 dias de análise, que levou em consideração o relatório técnico do produto (características de qualidade, dados de fabricação, controle de qualidade e estabilidade) e o relatório de experimentação terapêutica (ensaios não clínicos e clínicos).
"Essas avaliações são pautadas em marcos regulatórios e legislações vigentes, além de referências bibliográficas científicas, nacionalmente e internacionalmente reconhecidas. A Anvisa ainda participa dos mais importantes fóruns internacionais de discussão técnica, como do Conselho Internacional para Harmonização de Requisitos Técnicos de Produtos Farmacêuticos para Uso Humano (ICH, sigla em inglês).
Dessa forma, a Agência está alinhada com as principais diretrizes regulatórias internacionais e adota o estado da arte dos critérios técnicos e regulatórios para a aprovação de medicamentos no país, promovendo e protegendo a saúde da população brasileira", explica o diretor Romison Mota. Mais detalhes sobre a liberação serão divulgados em coletiva de imprensa, a partir das 17h30.
+ Crianças vacinadas contra gripe têm menos chances de ter sintomas graves de covid-19, diz estudo
Apesar da aprovação, o Brasil ainda não conta com doses da vacina da Pfizer/BioNTech disponíveis. O Ministério da Saúde diz que as negociações - iniciadas em maio de 2020 -estão "emperradas por falta de flexibilidade das empresas." De acordo com o governo, tanto Pfizer quanto Janssen (cujas negociações para a compra de doses também está paralizada) pedem ao Brasil, por exemplo, "garantias de pagamento e se resguardam de eventuais efeitos graves que as vacinas possam causar, entre outras dificuldades que nenhum outro fornecedor pediu."
Testes em gestantes e crianças
As empresas Pfizer e Moderna foram as primeiras a inserir crianças acima dos 12 anos em testes clínicos para suas vacinas contra covid-19, nos Estados Unidos. De acordo com o jornal The New York Times, a expectativa é que os primeiros resultados saiam no meio do ano. Dependendo do desempenho das vacinas nesse grupo, as companhias devem, então, testar em crianças mais novas.
Depois delas, outras empresas já iniciaram os testes nas crianças e adolescentes, como a vacina de Oxford AstraZeneca.
As farmacêuticas Pfizer e BioNTech também estão entre as pioneiras a testar a vacina contra a covid-19 em gestantes. A expectativa é que os primeiros resultados estejam disponíveis ainda em 2021.
Até o momento, a vacinação de grávidas não é recomendada, por conta da ausência de estudos que comprovem a sua segurança para gestantes e bebês. Ainda assim, a Agência Europeia de Medicamentos (EMA) emitiu um comunicado em que sugere que o uso da vacina da Pfizer/BioNTech deve ser considerado caso a caso para grávidas.
from Crescer https://revistacrescer.globo.com/Saude/noticia/2021/02/anvisa-concede-registro-definitivo-da-vacina-da-pfizer-empresa-ja-testa-imunizacao-de-criancas-e-gravidas-nos-eua.html
